Ácido quinurênico
| Kynurenic acid Alerta sobre risco à saúde | |
|---|---|
 | |
 | |
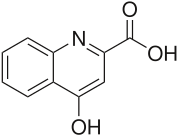
| Nome IUPAC | 4-hydroxyquinoline-2-carboxylic acid |
| Outros nomes | Ácido quinurênico, ácido quinurônico, transtorina |
| Identificadores | |
| Número CAS | 492-27-3 |
| PubChem | 3845 |
| ChemSpider | 3712 |
| KEGG | C01717 |
| ChEBI | 18344 |
| SMILES |
|
| InChI | 1/C10H7NO3/c12-9-5-8(10(13)14)11-7-4-2-1-3-6(7)9/h1-5H,(H,11,12)(H,13,14) |
| Propriedades | |
| Fórmula molecular | C10H7NO3 |
| Massa molar | 189.168 g/mol |
| Ponto de fusão | 282.5 °C, 556 K, 541 °F |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Ácido quinurênico (abreviado na literatura como KYNA ou KYN, de kynurenic acid) é um produto do metabolismo normal do aminoácido L-triptofano. Tem sido evidenciado que ácido quinurênico possui atividade neuroativa. Atua como um antiexcitotóxico e anticonvulsivo, provavelmente atuando como um antagonista nos receptores de aminoácidos excitatórios. Devido a esta atividade, pode influenciar importante processos neuropsicológica e neuropatológicos. Como resultado, ácido quinurênico tem sido considerado para utilização em terapêutica em certos distúrbios neurológicos. Por outro lado, o aumento dos níveis de ácido quinurênico também têm sido associadas a determinadas condições patológicas.[1][2]
Ácido quinurênico foi descoberto em 1853 pelo químico alemão Justus von Liebig na urina de cães, o que aparentemente produziu a posterior nomenclatura.[3]
É formada a partir de L-quinurenina, numa reação catalisada pela enzima transaminase quinurenina—oxoglutarato.
Referências
- ↑ Tonin, Anelise Miotti, et al; Inibição do metabolismo energético cerebral pelo ácido quinurênico em ratos jovens; Hospital de Clínicas de Porto Alegre. Semana Científica. (25. : 2005 set. : Porto Alegre, RS)
- ↑ César Augusto João Ribeiro; Efeito da Administração Intrastriatal Aguda de Ácido Quinolínico Sobre Metabolismo Energético em Ratos Jovens; Dissertação de mestrado apresentada ao Programa de Pós-Graduação em Ci~ências Biológicas-Bioquímica da Universidade Federal do Rio Grande do Sul, Porto Alegre, 2006.
- ↑ Liebig, J., Uber Kynurensäure, Justus Liebigs Ann. Chem., 86: 125-126, 1853.












